桐岐中期期中考试复习前五单元知识点
姓名: 班级:
第一、二单元
1、点燃蜡烛,将一只干冷的烧杯罩在火焰上方,烧杯壁有小水珠,说明蜡烛燃烧生成了 ;将小烧杯取下倒入少量澄清石灰水 ,变 ,说明蜡烛燃烧生成了 。该实验可说明,石蜡中一定含有的元素是 ,可能含有 元素。
2、托盘天平能称准到 克。称量干燥的固体时,要在两边托盘上各放一张干净大小相同的纸片,再称量;氢氧化钠要放玻璃器皿里称量,因为氢氧化钠易潮解,且有腐蚀性。称量时,药品放左盘。若称取25g氯化钠时,指针偏左,此时应 ,指针偏右,此时应 。
3、量取5毫升水要用 和 ,量液时,视线应与 保持水平。如仰视,读数比真实值偏 ,俯视,读数比真实值偏 。
4、少量试剂的反应在 里进行,较大量试剂的反应在 里进行。在常见的仪器中, 、燃烧匙、蒸发皿可直接加热, 、 不能直接加热,应放置在 上加热。
5、严谨的科学态度、合理的实验步骤、规范的操作方法是获得可靠实验结论的基本保证。
![C:UsersAdministratorAppDataRoamingTencentUsers249151849QQWinTempRichOleWODD}FXGD%O`PZQS6JK%]4S.jpg](https://yun.jsjyjy.net/player//data1/transform/2023/12/26/8/44/8380342AF2E79F4BE053113610AC360F/04520ad6771de2677cc9c76d58cc321b.doc/html4/transform.001.jpeg) 6、最早通过实验得出空气成分的科学家是法国的 。空气的成分按 计算,大约是:氧气占 ,氮气占 ,其他成分1%。空气属于 (物质类别)。
6、最早通过实验得出空气成分的科学家是法国的 。空气的成分按 计算,大约是:氧气占 ,氮气占 ,其他成分1%。空气属于 (物质类别)。
排放到空气中的 和 改变了空气的成分,造成空气污染,目前暂定为空气污染指数项目为 、 、 、 和 。
7、实验室用燃烧红磷法测定空气中氧气含量,现象是 , 水进入集气瓶内约占空气总体积的1/5,气体减少的体积小于五分之一的原因① ② ③装置未完全冷却就打开止水夹
8、混合物是由两种或两种以上物质混合而成的,这些物质之间没有发生化学反应。生活中常见的混合物如空气、溶液、合金、煤、石油、天然气;纯净物是指 ,例如:氧气、氢气、二氧化碳等 。
9、氧气能 ,可用于医疗急救,能 ,用于 、宇航等,氮气的化学性质 ,能用作食品包装袋内和灯泡中的 ,稀有气体有He、Ne、Ar等,化学性质很 ,常作 ,稀有气体可制成多种用途的电光源,是因为通电后能发出不同颜色的光,物理变化。
10、氧化反应是指 ;进行的慢不易被察觉的是 ,如食物变质、酿酒、钢铁生锈、 。
11、工业上制氧气的方法是 ,利用 不同,属于 变化。
12、在化学反应里能 其它物质的化学反应速率,而本身的 和 在化学反应前后
都没有发生变化的物质叫做 。催化剂所起的作用叫催化作用。
13、可作为过氧化氢分解的催化剂有 、硫酸铜溶液、 氧化铜、铁锈、红砖粉等
14、写出下列反应的符号表达式,在括号内写出基本反应类型
①黄色粉末在空气中燃烧,生成有刺激性气味的气体 。( )
②黑色固体在氧气中燃烧,生成气体使澄清石灰水变浑浊 。( )
③红色粉末在空气中燃烧,生成大量白烟 。( )
④黑色固体在氧气中剧烈燃烧,火星四射,生成黑色固体 。( )
⑤过氧化氢溶液中加入硫酸铜(CuSO4)溶液制氧气 。( )
⑥实验室用白色固体和黑色固体混合加热制氧气 。( )
⑦实验室用加热暗紫色固体制取氧气 。( )
⑧过氧化氢溶液中加入二氧化锰溶液制氧气 。( )
实验室制取气体
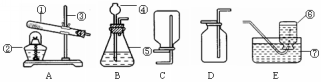
要点回顾:
a、发生装置的确定:若反应物的状态是 反应可选择A作为发生装置;
若是 反应,可选择B作为发生装置。
b、收集装置的确定:需要考虑气体的 和 ,若气体的密度大于空气,则可用
法收集,选用D装置;若气体的密度小于空气,则可用 法收集,选用C装置。若气体
难溶于水,不与水反应,则可用 法收集。
c、气体密度与空气密度的比较方法:空气的平均相对分子质量为29,若气体的相对分子质量
大于29,则密度比空气大,小于29,则密度比空气小。
(1)写出上图中标号仪器的名称① ② ③ ④ ⑤ ⑥ ⑦
(2)用过氧化氢和二氧化锰制取氧气可采用的发生装置是 ,其中二氧化锰起催化作用,反应的符号表达式为 ,可用 装置收集,原因是_ ,也可用 装置收集,原因是 。
(3)用A装置制取氧气,可选用氯酸钾作为原料,可以选择的装置组合为 或 ,
符号表达式 在A装置中添加 ,可选用 作为原料,缺少该
物品导致的后果是 。符号表达式
该实验的步骤大致有 ①把导管移出水面 ②点燃酒精灯加热 ③检查装置的气密性
④将反应物加入试管,用带有导管的橡皮塞塞紧并把它固定在铁架台上 ⑤排水法收集氧气 ⑥熄灭酒精灯。请按正确的操作顺序将以上步骤的序号写在横线上 。该装置中试管口必须略向下倾斜的原因是 。实验结束时,先 ,再 ,目的是防止 。检验氧气的方法是 。验满氧气的方法是 。
(4)实验室制取二氧化碳选用的原料大理石(或石灰石)、稀盐酸,方程式CaCO3 + 2HCl = CaCl2 + H2O + CO2↑若选用硫酸,导致的后果是反应一会停止,若选用浓盐酸,导致的后果是气体不纯,发生装置可选B,收集装置可选D。原因是二氧化碳密度比空气大且能溶于水。如何判断二氧化碳已经收集满了?在瓶口放一根燃着的木条,如果火焰熄灭说明已收集满。证明CO2用澄清石灰水,现象澄清石灰水变浑浊。反应的化学方程式为Ca(OH)2 + CO2 =CaCO3 ↓+ H2O
(5)实验室选用锌粒和稀硫酸作为原料来制H2,方程式为Zn + H2SO4 === ZnSO4 + H2↑
实验中可选择 作为发生装置, 或 作为收集装置,因为
(6)某学生用氯化铵固体和氢氧化钙固体加热反应制取氨气,可用的气体发生装置为 。
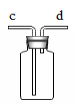
(7)若用右图用排空气法收集三种气体,则O2从 进,CO2从 进,H2从 进。
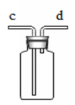
若用排水法收集H2,瓶内先装满水,气体从 端通入。
若用排水法收集O2,瓶内先装满水,气体从 端通入。
第三单元
1、原子是由居于原子中心的带 电的 和核外带 电的 构成的。原子核一般是由 和 构成,(但也有例外, 就没有中子)。原子中质子带 电,
中子 电,电子带 电。由于核内的 与核外的 相等,每个质子带一个单位的正电荷,每个电子 ,所以原子不显电性。
2、不同种类的原子中,核内的 不同,核外的 也不同;同一种原子中, =质子数= = ,但质子数不一定等于 。
3、原子的质量主要集中在 上,相对原子质量的符号为 ,Ar≈ + 。
4、为相对原子质量的测定作出卓越贡献的中国科学家是 。
5、元素是具有相同的 (即 )的一类原子的总称。决定元素种类的是 ,与元素化学性质关系密切的是 。
6、按质量计(填写符号)各种元素在地壳中的含量差别很大,前四位依次为 ;生物体内含量最多的金属元素是 ,含量最多的非金属元素是 ;海洋中含量最多的金属元素是 ,含量最多的非金属元素是 ;空气含量最多的非金属元素是 。人体中最多的物质是 。
7、元素符号表示 ,还表示这种元素的 ,例如,O即表示 ,又表示 ;3H表示 。
8、元素初步可以分为两类: 元素和 元素,如果细分,则还有一类是 元素,常温下呈液态的金属名称是 ,元素符号为 。
9、科学家 发现了元素周期表和元素周期律,元素周期表是按元素原子 核电荷数递增 的顺序排列的,共有 个横行, 18 个纵行。每一个横行叫做一个 ,每一个纵行叫做一个 (8、9、10三个纵行为一个 ),所以元素周期表共有 个周期, 个族。
10、元素周期表上对金属元素、非金属元素用不同的颜色做了分区,每周期开头的是 元素,靠近尾部的是 元素,结尾的是 元素。
11、构成物质的粒子有_ _、_ _和__ _,如:氧气由_ _(填微粒名称)构成,水由_ _ (填微粒名称)构成,水银由_ _(填微粒名称)构成,氦气由_ _(填微粒名称)构成,氯化钠由__ 和 (填微粒符号)构成,硫酸铜由__ 和 (填微粒符号)构成。
12、金属元素的原子最外层电子数目一般 4个,在化学反应中容易 电子,就带有 电荷,成为 离子; 非金属元素的原子最外层电子数目一般 4个,在化学反应中容易 电子,就带有 电荷,成为 离子.当 离子和 离子相互作用形成化合物时,整个化合物就 电性。
13、稀有气体元素的原子最外层有 个电子(氦有 个电子),这样的结构属于 结构.
14、写出下列离子符号:钠离子 镁离子 铝离子 氯离子
氢氧根离子 硝酸根离子 硫酸根离子 碳酸根离子 铵根离子
亚铁离子 铁离子 氢离子 氧离子 硫离子 氟离子
15、化学式可表示4个意义, 个宏观意义, 个微观意义。如过氧化氢的化学式为H2O2:则它的宏观意义分别是 、 ;它的微观意义分别是 , 。
16、请按顺序记忆1-20号的元素符号和元素名称
17、请背诵化合价口诀
 第四单元
第四单元
1、根据电解水实验装置图回答下列问题(“父亲大”):
(1)指出电源的正负极:A ;B ;
(2)C试管中为 气,D试管中产生的是 气;C、D两试管中气体的体积比是 ,分子个数比为 ,质量比为 。(5单元第5小题提示反应物质量比),该实验说明水是由 和 组成的,发生的化学反应的符号表达式为 ;
2、分子与原子的本质区别是___ _;分子又是由 构成的,一个水分子由 构成,一个五氧化二磷分子由 构成。
3、保持水化学性质的最小粒子是 。水加热变成水蒸气时,水分子 (填“变”或“不变”),只是 发生了改变,属于(填“物理”或“化学”) 变化;水电解时没有变化的粒子是 和 ,变化的粒子是 ,属于(填“物理”或“化学”) 变化。
4、由分子构成的物质中,混合物由 种分子构成,纯净物由 种分子构成;化合物
的分子由 种原子构成,单质的分子由 种原子构成。
5、物质的分子间有 ,气体容易压缩是因为其分子间的 ,液体、固体不易压缩,是因为其分子间的 。
6、天然水都不是纯净水,利用 、 、 和 等方法可以净化水,在净水操作中,常利用 溶于水后生成的胶状物吸附水中的杂质;除去污水中的泥沙等不溶性杂质,
可采用 的方法,在这个操作过程中常用到玻璃棒,其作用是 ,除玻璃棒外还要用到的仪器或用品有 _、 、 、 ;生产的自来水是 。(填纯净物或混合物)
7、区分硬水和软水的方法 。硬水可以通过物理或化学方法软化,生活中采用 、实验室采用 来降低水的硬度。区分纯水和矿泉水的方法取样,蒸发,有固体留下,是矿泉水,没有固体留下,是纯水 。
8、我们爱护水资源,一方面要 ,另一方面要 防止水污染
,水体污染的来源主要是 污染、 污染、 污染。
第五单元
1、 的 的 等于反应后生成的各物质的 这个规律就叫做质量守恒定律;该定律只适用于 。
2、在一切化学反应中,宏观上反应前后 没改变, 也没改变;微观上 没改变, 没增减, 也没改变。宏观上反应前后 一定改变,微观上 一定改变;宏观上反应前后 可能改变,微观上 可能改变。
3、书写化学反应方程式要遵守两个原则,一是 为基础,二是以要 。
4、用“一定不变”“可能变”“一定变”填空
在化学反应前后原子数目 ,原子种类 ,元素种类 ,物质的总质量 ,分子数目 ,物质种类 ,分子种类 。
5、电解水的化学方程式为2H2O 通电 2H2↑+ O2 ↑,该化学方程式表示的意义是(H;1 O:16 P:31):
① ;
② ;
③ 。
6、在4P + 5O2 点燃 2P2O5 反应中,每 份质量的P和 份质量的O2反应,生成 份 质量的P2O5
1