第六单元
1、 _是自然界里最硬的物质,可做 ,而_ _的质地较软,可做 ;用手触摸有 感,因此可做 ;它还有良好的_ 性,在干电池中作_ 。
2、焦炭、炭黑、木炭和活性炭都具有__ __的结构,因此都具有_ 性。防毒面具里的滤毒罐就是用活性炭来__ _ 的,制糖工业中也利用活性炭来_ 制白糖。
3、金刚石和石墨是由 直接构成,C60分子中60的含义是_ 。
4、金刚石、石墨和足球状的C60都是由碳元素组成的__ __,但它们的物理性质存在着差异,原因是_ __不同。
5、由金刚石、石墨和木炭的性质和用途可知,性质、结构和用途之间的关系是:
结构决定_ , 决定用途。
6、常温下,碳的化学性质 ,碳受日光照射或与 、 接触,都不容易起变化。古字画虽年久日深,仍不变色就是因为碳在常温下化学性质 。
7、碳在充足的氧气里燃烧生成 ,其反应的化学方程式为 ,在不充足的氧气里燃烧生成 ,其反应的化学方程式为 _。燃烧时都放出大量的_ 。
8、点燃一支蜡烛,把冷碟子放在蜡烛的火焰上方,过一会儿,能看到冷碟子的下面有_ ,这个实验说明蜡烛的成分里含有__ _元素。
9、二氧化碳的固体俗称___ _,它升华时要__ __,因此可用作_ __或用作_
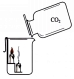 10、如右图所示的实验现象是 说明了二氧化碳具有的性质是_ _,_ __,且_ _。因此二氧化碳可用于 。
10、如右图所示的实验现象是 说明了二氧化碳具有的性质是_ _,_ __,且_ _。因此二氧化碳可用于 。
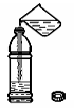
11、如右图所示,先在软饮料瓶中集满二氧化碳,再向瓶中加入约1/3瓶的水,盖紧瓶盖,振荡,观察到的主要现象是_ ,这个实验说明_ 。
12、如下图所示的实验是探究二氧化碳与水反应的实验。试将四朵用紫色石蕊染成的紫色干燥小花显示的颜色填入下表中,并回答有关问题:

| (Ⅰ) | (Ⅱ) | (Ⅲ) | (Ⅳ) | 烘干IV后 |
小花显示的颜色 |
|
|
|
|
(1)实验Ⅰ说明的问题是__ _;实验II说明的问题是__ __;实验III说明的问题是 ;
(2)整个实验说明的问题是 __,实验Ⅳ中发生反应的化学方程式是_ ;(3)如果将实验Ⅳ后的小花小心烘烤,又能观察到的现象是_ ,这个现象说明 ,烘烤时发生反应的
化学方程式__ 。
13、温室效应使全球气候变暖,能产生温室效应的气体有 、 _、
和氟氯代烷__等。人类只有一个地球,为了保护人类赖以生存的环境,防止温室效应的进一步加强,人类应减少使用_ 、 、 等化石燃料,更多地利用太阳能_、风能、地热等清洁能源,大力植树造林,严禁乱砍滥伐等。
14、一氧化碳具有可燃性,在炭火的上方和煤炉的上方的 _,就是一氧化碳在燃烧,所以一氧化碳是许多气体燃料的主要成分。一氧化碳燃烧的化学方程式是_ 。现象: 。
15、一氧化碳具有毒性,是因为它能与 _结合,造成生物体内缺氧,严重时危及生命。
16、一氧化碳和木炭一样具有还原性,能使氧化铜还原成 ,同时生成_ _。该反应的化学方程式是 _。
17、CO2与CO化学性质存在较大差异的原因是
18、在O2、N2、H2、CO、CO2、CH4中选择适宜的化学式填入下列各题的横线上:
(1)密度比空气大的气体是 (2)具有可燃性的气体是
(3)燃烧后产生使澄清石灰水变浑浊的气体 (4)能用来作保护气的气体是
(5)能用来灭火的气体是 (6)具有助燃作用的气体是
(7)最轻的气体是 (8)能使紫色石蕊溶液变红的是
(9)吸烟过程中,产生的一种与血红蛋白结合的有毒气体是

第七单元
1、(1)右图是燃烧条件示意图:请根据初中所学知识,写出燃烧的三个条件:
① ② ③
(2)物质发生化学反应的同时,伴随着能量的变化,通常表现为 的变化,有的反应 ,有的反应 。人类通过化学反应获得的能量,大多来自于化石燃料。石油是化石燃料之一,属于_ (填“纯净物”或“混合物”)。
(3)奥林匹克火炬(内部储有可燃物)是奥林匹克圣火的载体。采集奥林匹克圣火的唯一方式,是在奥林匹克的赫拉神庙前通过太阳光集中在凹面镜的中央,引燃圣火。此过程中最关键的燃烧条件是 。
(4)5月8日,北京奥运会“祥云”特制火炬克服低温、低压、空气稀薄、大风等不利条件,在珠峰之巅燃烧,举世为之惊叹。普通火炬在珠峰恶劣气候条件下易熄灭原因是:
① 温度降到了着火点以下 ② 氧气的浓度太低 (答两条即可)。
2、灭火的原理是① 清除可燃物或使可燃物与其他物品隔离 或② 隔绝氧气(或空气)
或③ 。
3、放热反应有:Mg+2HCl=MgCl2+H2↑ 、
4、化石燃料有 、 石油 、 ,它们是 不可 再生能源。
工业的“粮食”是指: 煤 ,工业的“血液”是指 石油 。
5、煤是复杂的 混合物 (填“混合物”或“纯净物”),主要含 碳 元素,煤燃烧时会排放出 、 等污染物,这些气体溶于雨水,会形成 ,其危害有 ,影响作物生长,影响人体健康 。将煤隔绝空气加强热分解成焦炭、煤焦油、煤气等,这一过程是 变化,得到煤气的主要成分是 H2 、 CH4 、 。
6、石油是混合物(填“混合物”或“纯净物”),主要含有 C 、 H两种元素,石油炼制利用各成分的沸点不同进行分离,是 变化。
7、工农业生产和生活中经常考虑使燃料充分燃烧的两点是一、
二、 。
工业上燃烧固体煤的时候,为了使使燃料与空气有足够大的接触面积,通常采取的措施
把煤块加工成煤粉 ;日常燃烧固体煤的时候,通常采取的措施是 做成蜂窝煤 。
8、压缩天然气加油站的标志字母是 ,液化石油气加油站标志字母是 。
9、化石燃料中 天然气 是比较清洁的燃料,天然气、沼气、瓦斯中的主要成分都是 。
瓦斯爆炸反应的方程式_
10、乙醇俗称 酒精,化学式为 ,燃烧的化学方程式为
11、实验室制取氢气的原料是 和 ,反应的化学方程式是 。
12、氢气是一种理想的新能源,其具体的优越性为 ① 放热多 ② ③ 原料来源广、是可再生能源 。但由于 , 目前,氢气还没有推广使用。随着科技的发展,氢气一定能成为人类社会的主要能源。燃烧反应的化学方程式为
13、泡沫灭火器反应原理是
14、请设计实验鉴别下列物质氢气、一氧化碳和甲烷 取样,分别点燃,先用干冷小烧杯罩在火焰上方,再将用石灰水润湿过的烧杯罩在火焰上方,既有水雾又有浑浊的是甲烷,只有水雾的是氢气,只有浑浊的是一氧化碳。
第八单元
1、金属材料包括 和 。铁、铝等大多数金属都呈银白色,但铜却呈 ,金呈黄色;在常温下,铁、铝、铜等大多数金属都是固体,但体温计中的汞却是 。
2、地壳中含量最多的是金属元素是 ;导电性、导热性最好的金属是 ;人体中含量最多的金属是 ;涂在保温瓶胆夹层内的银白色金属是 ;做普通干电池负极的金属是 ;体温计中的金属是 用来做人造骨的是(名称) 。硬度最大的金属是 ;熔点最高的金属是 。
3、在金属中加热熔合某些 或 而制得合金,铁的两种常见合金是 和 ,
它们的性质不同是因为 ,百炼成钢的方程式是
4、合金的强度和硬度一般比组成它们的纯金属 ,抗腐蚀性能等也更好,合金的熔点一般比组成它的纯金属 。
5、淬火和回火是金属热处理中的常用的两种方法。例如,经过淬火后的钢,其硬度和耐磨性增强,塑性和韧性却 。淬火的钢再经回火后, 部分恢复。
6、“真金不怕火炼”的含义是 金即使在高温下也不和氧气反应
7、金属的化学性质
(1)金属与 氧气 反应。如 :
①铝的化学性质活泼,但铝制品通常耐腐蚀。因为其表面生成致密的氧化铝 薄膜,化学方程式是 。不宜用钢刷来擦洗铝制品的是因为破坏保护膜,制品不耐用 。
②照明弹原理2Mg + O2 ![]() 2MgO
2MgO
(2)活泼(①Fe 、②铝和盐酸、硫酸反应)金属与酸反应。如:
①市场上出售的补血麦片中常含有微量颗粒细小的还原性铁粉,与人体胃液中的盐酸反应转化为亚铁盐,起到补血作用,这个反应的化学方程式
② 、 。
(3)金属与盐溶液反应。如:
①铝丝浸入硫酸铜溶液中,方程式 ,观察到铝丝表面有 , 色溶液变为 色。
②把红色的铜丝浸入无色的硝酸银溶液中,方程式 ,实验中可观察到铜丝表面有 色固体出现,溶液由 色变为 色。
③不用铁制容器盛放波尔多液(含有硫酸铜)的理由用方程式表示 。
8、工业炼铁的原料是 、 、 把它们一起放入炼铁的设备 中,在高温条件下,利用 焦炭与氧气生成的CO 把铁从铁矿石中还原出来。
9、用赤铁矿炼铁的方程式 。现象是 、
。用磁铁矿石来炼铁的方程式
现象是固体仍为 、 。
10、保护金属资源的有效途径是: 、 、合理有效地开采矿物 、 寻找金属的代用品 。
11、铝与氧气反应生成的 的氧化铝薄膜,覆盖在铝表面,从而保护里层的铝不再与氧气反应;而铁与 、 等反应生成的铁锈却很 ,不能阻碍里层的铁继续与氧气与水蒸气等应,因此铁制品可以全部被锈蚀。铁锈的主要成分是 。自行车的构件如支架、链条、钢圈等,分别采取了什么防锈措施? ; ;镀其它金属。
第九单元
1、写出下列溶液中的溶质、溶剂或溶液的名称:
溶液 | 盐酸 | 硫酸铜 溶液 | 澄清石灰水 | 氢氧化钠 溶液 | 碘酒 | 75%的消毒酒精 |
溶质 |
|
|
|
|
|
|
溶剂 |
|
|
|
|
|
|
2、 能溶解很多种物质,是一种最常用的溶剂。汽油、酒精等也可以做溶剂,如汽油能溶解 ,酒精能溶解 。把药品配成溶液再做实验的目的是 、 。
3、物质在溶解于水的过程中通常伴随着热量的变化:有些物质在溶解时会出现放热现象,如 ;有些物质在溶解时会出现吸热现象,如 ;有些物质在溶解时温度基本保持不变,如 。
4、同种物质的饱和溶液与不饱和溶液是可以相互转化的。
(1)对于大多数物质来说,由饱和溶液转化为不饱和溶液的方法是 、
 (2)对于大多数物质来说,由不饱和溶液转化为饱和溶液的方法: ; ; 。
(2)对于大多数物质来说,由不饱和溶液转化为饱和溶液的方法: ; ; 。
5、打开汽水瓶盖时,汽水会自动喷出,这说明: , 。_
喝了汽水后,常常会打嗝,这说明: , 。
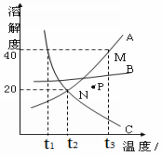
6、右图是A、B、C三种物质的溶解度曲线看图回答:
①M点表示 。
②N点表示 。
③t1℃时,这三种溶解度由小到大的排列顺序是 。
④t3℃时,用等质量的水配制的三种物质的饱和溶液,若降温至t1℃,
有溶质析出的是 ,析出量较多的是 。此时溶液中溶质质
量分数由小到大的顺序是: 。
⑤欲从接近饱和的B溶液中得到B,通常采用 的方法。
欲从接近饱和的A溶液中得到A,通常采用 的方法。
欲将A从A、B的混合物(B少量)分离出来,可采用 的方法。
⑥t3℃时,将50克A加入50克水中,充分搅拌后,可得到A溶液 克。
⑦一定温度下,现有质量相同的水配制而成的A、B、C三种物质饱和溶液,降温后,有溶质析出的是__ ___,析出较多溶质的是__ ___,溶液从饱和变为不饱和的是__ 。
⑧对于图中P点,A溶液属于 (饱和溶液或不饱和溶液,下同);B溶液属于
;C溶液属于
7、将不饱和的氢氧化钙溶液变为饱和溶液的方法是: ; ; 。
考前必备
一、符号的意义
1、数字“2”的意义
2O: 2O2:前2 后2 2O2-:前2 后2
![]() :
: ![]() :
:
2、化学式的意义,如:C6H12O6
(1)
(2)
(3)
(4)
3、化学方程式的含义,如:2H2O ![]() 2H2↑+ O2 ↑
2H2↑+ O2 ↑
(1)
(2)
(3)
二、物质分类
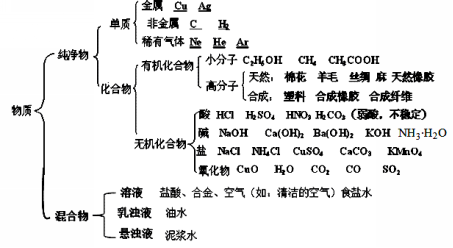
基础化学方程式
1、实验室制氧气:
①加热氯酸钾(少量的二氧化锰):
②过氧化氢分解(二氧化锰作催化剂):
硫酸铜溶液作催化剂:
③加热高锰酸钾:
2、工业制氧气: 分离液态空气法(物理变化) (根据N2和O2的 不同,氮气的沸点比氧气低)
3、实验室制二氧化碳:大理石(或石灰石)与稀盐酸反应:
4、工业制二氧化碳:高温煅烧石灰石:
5、实验室制氢气:锌和稀硫酸反应:
![]()
化合反应:多种物质生成一种物质 3Fe + 2O2 ![]() Fe3O4
Fe3O4
6、化学反应四种 分解反应:一种物质生成多种物2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
基本反应类型 置换反应:单质和化合物反应生成单质和化合物
Cu + 2AgNO3=Cu(NO3)2 + 2Ag
C + 2CuO ![]() 2Cu + CO2↑
2Cu + CO2↑
复分解反应(11单元在学习):两种化合物相互交换成分化合价不变生成两种新的化合物 (中和反应属于复分解反应)
化学实验操作
一、过滤
过滤操作中注意点
“一贴”:
“二低”: 、
“三靠”: 、 、
(1)如果过滤后仍然浑浊,可能是由于什么原因?
(2)用此法 降低水的硬度(填“可以”或者“不可以”),生活中用来降低水的硬度的方法是 ,实验室用来降低水的硬度的方法是
(3)(11单元学习)粗盐中含有可溶性杂质如CaCl2、MgCl2 Na2SO4等,也含有难溶性杂质泥沙等,粗盐提纯的目的就是除掉不溶性杂质,可采用溶解、过滤、蒸发的方法。三次操作中都要用到玻璃棒,其作用分别是加速溶解、引流、防止液滴飞溅,蒸发时,当出现较多固体时停止加热。(用余热蒸干)
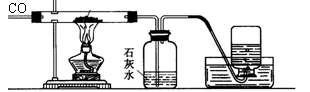 二、冶炼金属原理
二、冶炼金属原理
(1)若试管中装CuO,可观察到的现象是 , ,反应方程式为
(2)若试管中的物质是Fe2O3,可观察到的现象是 , ,反应方程式为
(3)该实验说明CO具有 性。在这两个实验中都应该先通 后 ,目的是 ,实验结束后集气瓶中的气体要进行处理,原因是 。可采用 的方法处理CO。 注意实验顺序:通气→加热→停止加热→停止通气
(4)若试管中装的是Fe3O4,可观察到的现象是澄清石灰水变浑浊,反应方程式为
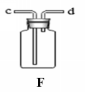
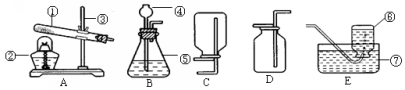
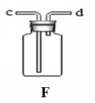
实验室制取气体
要点回顾:
a、发生装置的确定:若反应物的状态只有固体并在加热条件下反应则可选择 作为发生
装置;若是反应物中只要有液体,且常温下反应,则选择 作为发生装置。
b、收集装置的确定:需要考虑气体的密度和溶解性,若气体的密度大于空气,则可用 法收集,选用 装置;若气体的密度小于空气,则可用 法收集,选用 装置。
若气体难溶于水,不与水反应,则可用 法收集。
c、气体密度与空气密度的比较方法:空气的平均相对分子质量为29,若气体的相对分子质量
大于29,则密度比空气 ,小于29,则密度比空气 。
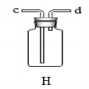
d.如果用如图F所示装置作排水法收集氧气,应先在F装置中 ,氧气应从 (填“c”或“d”)端导入,如用F装置收集二氧化碳 (填“c”或“d”)端导入, 检验F装置中二氧化碳是否集满的方是 ;如要检验某气体是否为二氧化碳的方法是 。
1 写出图中标号仪器的名称① ② ③ ④ ⑤
⑥ ⑦
(2)实验室制氧气
① 用过氧化氢和二氧化锰制取氧气可采用的装置组合是 或 ,其中二氧化锰起 作用,
反应的化学方程式为 ,
若滴入CuSO4溶液,方程式为
② 用A装置制取氧气,选用 作为原料,二氧化锰做催化剂,装置组合为 或 ,
化学方程式
③ 在A装置中添加 ,可选用 作为原料,缺少棉花导致的后果是 ,方程式为 。
该实验的步骤大致有 ①把导管移出水面 ②点燃酒精灯加热 ③检查装置的气密性 ④将反应物加入试管,用带有导管的橡皮塞塞紧并把它固定在铁架台上 ⑤排水法收集氧气 ⑥熄灭酒精灯。请按正确的操作顺序将以上步骤的序号写在横线上 。该装置中试管口必须略向下倾斜的原因是 。
④ 用排水法收集氧气,检验氧气已经收满的方法: 。
⑤ 用向上排气法收集氧气,检验氧气已经收满的方法: 。
2 实验室制取二氧化碳选用的原料 、 ,
化学方程式 ,发生装置只选 ,收集装置只选
若选用硫酸,导致的后果是 ,
若选用浓盐酸,因为 ,导致 ,若通入石灰水,则石灰水 。
如何判断二氧化碳已经收集满了? 。证明收到的气体是CO2方法:
3 实验室选用 和 作为原料来制H2,方程式为
实验中可选择 作为发生装置, 收集装置。
⑸某学生用氯化铵固体和氢氧化钙固体加热反应制取氨气,可选用的气体发生装置为A
注意:
1、课外实验
(上册) P77 P112 P122
(下册) P7 P39 P45 P58 P110
2、关注所有插图
3、上册:实验室图标 燃烧、爆炸图标
下册:塑料包装制品回收标志
4、资料卡片、方法引导
1
评论
还能输入140字
用户评论